Anvisa recebe pedido de autorização para estudos de fase 3 para a vacina Covaxin
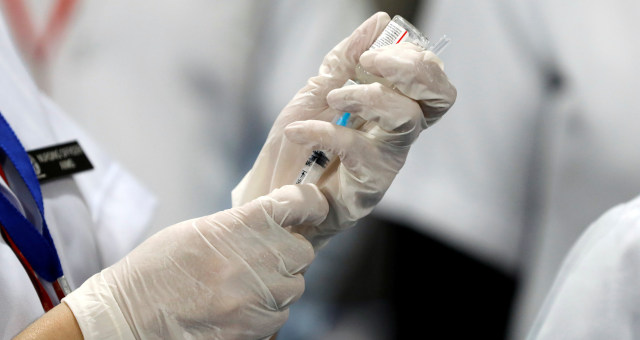
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu nesta sexta-feira pedido de autorização para a realização de estudos clínicos de fase 3 no país para a vacina Covaxin, desenvolvida pelo laboratório indiano Bharat Biotech.
Segundo comunicado da Anvisa, o pedido foi feito pela Precisa Farmacêutica, que é parceria do Bharat Biotech no Brasil.
A Avisa disse que tem de três a cinco dias para a análise do pedido, “condicionada a apresentação dos dados necessários para a análise técnica”. A avaliação da agência reguladora visa verificar se a proposta é capaz de “gerar dados confiáveis sobre a segurança e eficácia da vacina”.
A terceira fase dos estudos clínicos é a etapa em que são realizados testes com seres humanos.
Na quarta-feira, a Anvisa decidiu flexibilizar exigências para pedido e aprovação de uso emergencial de vacinas contra Covid-19 no país e anunciou que vai liberar, sob determinadas circunstâncias, a utilização de imunizantes não testados em fase 3 no Brasil.
![[Conteúdos gratuitos] Assista ao Giro do Mercado e outros programas exclusivos em nosso Youtube](https://www.moneytimes.com.br/uploads/2024/01/banner-html-28.png)











